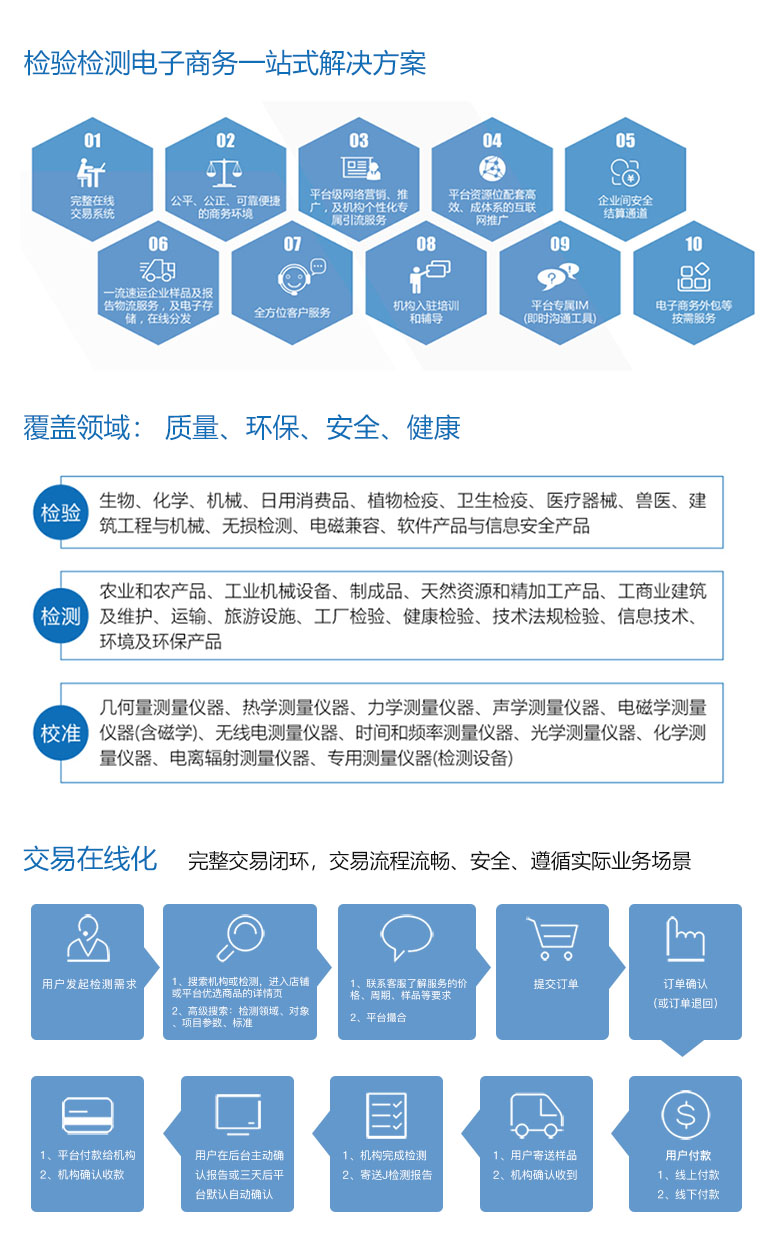
完整交易系统
流畅、安全;遵循实际业务场景
植入后局部反应试验 GB/T 16886.6-2015、医用输液、输血、注射器具检验方法:GB/T 14233.2-2005、医用有机硅材料生物学评价试验方法 GB/T 16175-2008、植入后局部反应试验 ISO 10993-6:2016、牙科学牙科医疗器械生物相容性评估 ISO 7405-2018、皮下植入试验 YY/T 0127.8-2001、试验方法骨埋植试验 YY/T 0127.4-
由
优检联优选
提供服务
商品ID:524314067814075502
价格
¥81000.0-81000.0
已订购
服务周期: 60天
选择推荐套餐有优惠,或者直接自选检测项目,如有疑问请咨询客服
测试标准/方法:
样品规格:

橡胶-轮胎橡胶检验裂解-GA/T 1516-2018
法庭科学领域,轮胎橡胶,裂解,气相色谱、质谱

血液、尿液-《生物检材中苯丙胺类兴奋剂、哌替啶和氯胺酮的测定》-SF/Z JD0107004-2016
哌替啶/甲基苯丙胺/苯丙胺

油脂及残留物、火灾现场助燃剂、残留物-微量物证-GB/T 19267.7-2008
气相色谱质谱法,适用于刑事技术领城中微量物证的理化检验

血液、尿液-《生物检材中单乙酰吗啡、吗啡、可待因的测定》-SF/ZJD0107006-2010
血液、尿液、组织及毛发中单乙酰吗啡、吗啡和可待因的免疫筛选法、气相色谱-质谱联用法和液相色谱-串联质谱法

橡胶-橡胶鉴定-GB/T 7764-2017
《橡胶鉴定红外光谱法》,生胶、硫化胶、未硫化胶、及热塑性弹性体,定性分析
医疗器械生物学评价第6部分:植入后局部反应试验 GB/T 16886.6-2015;

医用输液、输血、注射器具检验方法第2部分:生物学试验方法 GB/T 14233.2-2005;
本部分规定了医用输液、输血、注射器具生物学试验方法。
本部分适用于医用输液、输血、注射器具。
医用有机硅材料生物学评价试验方法 GB/T 16175-2008;
本标准规定了医用有机硅材料的生物学评价试验方法。
本标准适用于医用有机硅材料的生物学评价。
医疗器械生物学评价第6部分:植入后局部反应试验 ISO 10993-6:2016;
ISO 10993- 6:16 16规定了用于医疗设备的生物材料植入后局部效应评估的测试方法。
ISO 10993- 6:16适用于:固体和不可吸收,非固体,如多孔材料、液体、凝胶、膏体和微粒、可降解和/或可吸收,可固体或非固体。
牙科学牙科医疗器械生物相容性评估 ISO 7405-2018;
本文件规定了用于牙科的医疗设备生物效应评估的测试方法。它包括药理学药剂的测试,这些药剂是被测设备的一个组成部分。
本文件不包括不直接或间接接触患者身体的材料和设备的检测。
口腔医疗器械生物学评价第2单元:皮下植入试验 YY/T 0127.8-2001;
本标准规定了口腔材料的皮下组织植入试验方法。
本标准适用于评价长期与口腔组织接触的口腔材料对皮下组织的反应。
口腔医疗器械生物学评价第2单元:试验方法骨埋植试验 YY/T 0127.4-2009
本标准规定了口腔医疗器械的骨埋植试验方法。
本标准用于评价骨组织对拟长期与口腔骨组织接触的口腔医疗器械的生物学反应。

完整交易系统
流畅、安全;遵循实际业务场景
安全便捷支付
支持线上线下多种支付方式
专业资质审核
安全可信赖检测机构
数据查询追踪
全程服务全程跟进